Akut Miyeloid Lösemi (AML)
Akut Miyeloid Lösemi hematopoietik kök hücrelerdeki genetik değişiklikler sonucu ortaya çıkar. Bu rahatsızlık özellikle FLT3 NPM1 ve TP53 genlerinde mutasyon içerir. Hastalık kemik iliği ve kanı anormal beyaz kan hücreleriyle doldurur. Bu hücrelerin olgunlaşmaması kan üretimini ciddi şekilde bozar.
Ayrıca AML tedavisinde son zamanlarda önemli ilerlemeler kaydedilmiştir. Özellikle FLT3 ve IDH inhibitörleri gibi hedefli terapiler bazı hasta gruplarında sağkalım sürelerini uzatmayı hedeflemektedir. Dolayısıyla bu tedaviler hastalığın seyrini ve tedaviye verilen yanıtları büyük ölçüde etkiler.
| Tanım | Kemik iliğinde anormal myeloid hücrelerin hızlı şekilde çoğalmasıyla oluşan ve olgunlaşmamış hücrelerin (blastlar) kanda ve kemik iliğinde birikmesine yol açan bir tür kan kanseridir. Hızlı ilerler ve acil tedavi gerektirir. |
| Nedenleri | Çoğunlukla nedeni bilinmez, ancak genetik mutasyonlar, kimyasal maruziyet (benzen), radyasyon, bazı kemoterapi ilaçları, myelodisplastik sendromlar ve bazı genetik bozukluklar (Down sendromu gibi) AML riskini artırabilir. |
| Belirtiler | Yorgunluk, solukluk (anemi), sık enfeksiyonlar (düşük beyaz kan hücreleri), kolay morarma ve kanamalar (düşük trombositler), kemik ve eklem ağrısı, ateş, kilo kaybı, lenf düğümlerinde şişme |
| Tanı Yöntemleri | Tam kan sayımı (CBC), periferik kan yayması, kemik iliği biyopsisi, sitogenetik testler, moleküler genetik analizler (mutasyon tespiti için), akım sitometrisi |
| Tedavi Yöntemleri | İndüksiyon tedavisi: Yoğun kemoterapi ile blast hücrelerin azaltılması. Konsolidasyon tedavisi: Kemoterapi, allojenik kök hücre nakli (yüksek riskli hastalarda) |
| Yan Etkiler | Kemoterapiye bağlı bulantı, kusma, saç dökülmesi, yorgunluk, enfeksiyon riski, anemi, kanama, uzun dönem kemik iliği baskılanması |
| Süre | Tedavi süresi birkaç ay ila bir yıl arasında değişebilir; yoğun kemoterapi sonrası remisyon elde edilebilir, ancak bazı vakalarda tekrarlama riski vardır. |
| Kullanılan İlaçlar | Sitarabin, daunorubisin, idarubisin, mitoksantron (kemoterapi ajanları), midostaurin (FLT3 mutasyonu olan hastalar için), enazitinib (IDH2 mutasyonu olan hastalar için) |
| Avantajları | Yoğun tedaviyle remisyona girme ve hastalığın kontrol altına alınma şansı; bazı hastalarda kök hücre nakli ile tam iyileşme sağlanabilir |
| Dezavantajları | Tedaviye rağmen hastalığın tekrarlama riski; yoğun kemoterapiye bağlı ciddi yan etkiler ve enfeksiyon riskleri; kök hücre nakli sonrası greft-versus-host hastalığı riski |
| İzlem ve Kontrol | Düzenli kan testleri ve kemik iliği biyopsileri ile remisyon durumu izlenir; tedavi sonrası nüks riskine karşı uzun süreli takip gerekir |
| Alternatif Tedaviler | Klinik denemeler (yeni ilaçlar ve hedefe yönelik tedaviler), immünoterapi, CAR-T hücre tedavisi, yeni nesil genetik mutasyon inhibitörleri |

Doç. Dr. Mahmut Bakır Koyuncu
Mersin doğumlu, YKAL mezunu. 2011 yılında Hacettepe Üniversitesi Tıp Fakültesinden mezun olmuştur. İç Hastalıkları anadal ve Hematoloji yandal eğitimlerini Mersin Üniversitesi Tıp Fakültesinde tamamlamıştır. 2008 yılında MD Anderson Cancer Center’da moleküler biyoloji ve genetik alanında çalışmış, 2020 yılında New York Presbyterian Hospital’da kemik iliği nakli ve hücresel tedaviler ünitesinde çalışma imkanı bulmuştur. Türkiye’ye döndükten sonra sırasıyla Mersin Şehir Hastanesi ve Adana Şehir Eğitim ve Araştırma Hastanesinde çalışmıştır. 2022’de Hematoloji alanında Doçent Doktor unvanı almıştır. Temmuz 2023’ten beri Mersin Medical Park Hastanesinde çalışmaktadır.
Akut Miyeloid Lösemi Nedir?
Akut Miyeloid Lösemi blast adı verilen olgunlaşmamış myeloid hücrelerin hızla çoğalmasıyla tanımlanır. Bu hızlı çoğalma periferik kanda ve kemik iliğinde gözlemlenir. Hastalığın ilerlemesiyle kemik iliği yetersizliği meydana gelir ve bu da eritropoez ile megakaryopoez süreçlerini olumsuz etkiler. Sonuç olarak kırmızı kan hücreleri ve trombositlerin üretimi azalır.
Akut Miyeloid Lösemi’nin tedavisinde çoklu ajan kemoterapisi önemli bir rol oynar. Tam remisyon elde edilse de çözüm allojenik kök hücre naklidir. Bu tedavi hastalığın kontrol altına alınmasında kritik bir öneme sahiptir. Ancak prognoz özellikle yaşlı hastalarda hâlâ zorlayıcıdır. Tedavi stratejilerindeki ilerlemeler hastalığın yönetimini iyileştirmeye devam etmektedir.
Akut Miyeloid Lösemi Nedenleri Nelerdir?
Akut Miyeloid Lösemi çeşitli etkenlerin birleşimi sonucunda gelişir. Genetik mutasyonlar bu hastalığın temelini oluştururken çevresel faktörler ve öncül sağlık durumları da riski artırabilir. Miyelodisplastik sendromlar gibi önceden mevcut durumlar sık sık AML’nin habercisi olabilir. Özellikle yüksek ve çok yüksek riskli MDS hastaları bu kansere evrilebilir.
Hematolojik bozukluklar da AML riskini artırır:
- Miyelofibroz
- Esansiyel trombositemi
- Polisitemi vera
- Kronik miyeloid lösemi
Bu hastalıklar miyeloproliferatif neoplazmlar kategorisinde yer alır ve AML’ye ilerleme eğilimindedir. Bu durumlar genellikle klinik fenotipin başlangıç özelliklerine göre farklılaşır. Trombositemi olan hastalarda örneğin yüksek trombosit sayıları gözlemlenir. Bunun yanı sıra genel kan sayımında azalma ve periferik blastlarda artış yaygın bir bulgudur.
Ek olarak geçmişte başka kanser türleri için yapılan kemoterapi de AML gelişim riskini artırabilir. Özellikle alkilleyici ajanlar ve radyasyon maruziyeti sonrası MDS/AML oluşumu mümkündür. Bu tür durumlar genellikle tedavi sonrası 5 ile 7 yıl arasında ortaya çıkar. Topoizomeraz inhibitörleri de benzer risk taşır ve genellikle 11q23 yeniden düzenlemeleri ile ilişkilidir.
Çevresel faktörler de AML riskine katkıda bulunur:
- Radyasyon
- Tütün dumanı
- Benzen
Bu bilinen risk faktörlerine rağmen birçok AML vakası hala belirsiz nedenlerle ortaya çıkar. Bu karmaşık etkileşim hastalığın anlaşılmasını ve yönetilmesini zorlaştırır.
*En iyi şekilde geri dönüş yapabilmemiz için tüm alanları doldurmanızı öneririz.
Akut Miyeloid Lösemi Ne Kadar Yaygındır?
Akut Miyeloid Lösemi her yıl Amerika Birleşik Devletleri’nde 20.000’den fazla yeni vaka ile görülmektedir. Bu hastalık erkeklerde kadınlardan daha yaygındır; erkeklerde görülme oranı kadınlara oranla 5:3’tür. Ortanca teşhis yaşı 68 olarak saptanmıştır bu da AML’nin özellikle yaşlı nüfusta daha sık rastlanan bir durum olduğunu gösterir. Yine de bu kanser türü hem erkekleri hem de kadınları etkileyebilmekte yıllık insidans oranı 100.000 nüfus başına yaklaşık 4,3’tür. Hispanik olmayan Beyaz nüfusta ise daha yüksek bir yaygınlık gözlemlenir. Bu istatistikler AML’nin toplumda ne kadar yaygın olduğunu açıkça ortaya koymaktadır.
Akut Miyeloid Lösemi Sırasında Neler Olur?
Akut Miyeloid Lösemi sırasında hastalığın temeli olan patolojik süreçler karmaşık bir dizi etkileşimden oluşur. Hastalık kemik iliği kompartmanında farklılaşmamış myeloid öncülerin kontrolsüz çoğalmasıyla karakterizedir. Bu hücreler genetik ve sitogenetik anormalliklerin birikimi sonucu klonal olarak çoğalır. Bu çoğalma kemik iliği yetmezliğine ve etkisiz kan hücreleri üretimine yol açar.
Hastalık sürecinde meydana gelen çeşitli genetik anormallikler AML’nin sınıflandırılmasında temel rol oynar:
Uygun riskli AML:
- t(8;21)(q22;q22.1) kromozomal translokasyonu
- inv(16)(p13.1q22) kromozomal değişiklik
- FLT3-ITD mutasyonu olmayan mutasyona uğramış NPM1 veya CEBPA mutasyonlarına sahip hastalar
Orta riskli AML:
- Herhangi bir FLT3-ITD mutasyonu
- t(9;11)(p21.3;q23.3) veya MLL
- yeniden düzenlemesi
Yüksek riskli AML:
- Monosomi 5/del 5q veya 7/delesyon 7q
- Diğer monosomal veya kompleks karyotip (≥3 ilgisiz anormallik)
- ASXL1, EZH2, SRSF2 veya TP53 mutasyonları
Hastalığın seyri boyunca RUNX1 gibi belirli genler AML’nin gelişiminde ve ilerlemesinde önemli rol oynar. Özellikle t(8;21)(q22;q22) AML’si formunda etkili olan RUNX1 hematopoezin kritik bir parçasıdır ve genellikle dirençli hastalık formlarıyla ilişkilendirilir.
İzokitrat dehidrojenaz (IDH) mutasyonları da AML’nin patogenezi içinde yer alır. Bu mutasyonlar onkojenik etkiler sergileyerek hastalığın ilerlemesini hızlandırır ve genellikle daha yaşlı bireylerde görülür.
Son olarak TP53 mutasyonları özellikle kötü prognostik faktörler arasında yer alır ve bu mutasyonlara sahip hastalar genellikle kemoterapiye direnç gösterir. Bu direnç tedavi stratejilerinin yeniden değerlendirilmesini gerektirir.
Akut Miyeloid Lösemi Belirtileri Nelerdir?
Akut Miyeloid Lösemi belirtileri genellikle hızla ortaya çıkar ve hastaların günlük yaşamlarını etkiler. Etkisiz eritropoez sonucu anemi yorgunluk ve nefes darlığı gibi semptomlar gelişir. Ayrıca hastalar kolay morarma ve aşırı kanama gibi kanama bozukluklarından muzdarip olabilirler. Tekrarlayan enfeksiyonlar da AML’nin yaygın işaretlerindendir.
Fizik muayenede soluk cilt ve morarmalar dikkat çekerken karaciğer ve dalak büyümesi olan hepatosplenomegali saptanabilir. Nadiren lenf bezi büyümeleri lenfadenopati şeklinde gözlemlenebilir. Ayrıca miyeloide eşdeğer myeloid sarkom deride kalınlaşmış ve koyu renkli lezyonlarla kendini gösterir. Genellikle ağız mukozasında kanamalar ve cilt altında noktasal kanamalar görülebilir. Hastalık damar içi pıhtılaşma sorunlarına yol açabilir bu durum ciddi komplikasyonlara neden olabilir.
Akut Miyeloid Lösemi Nasıl Teşhis Edilir?
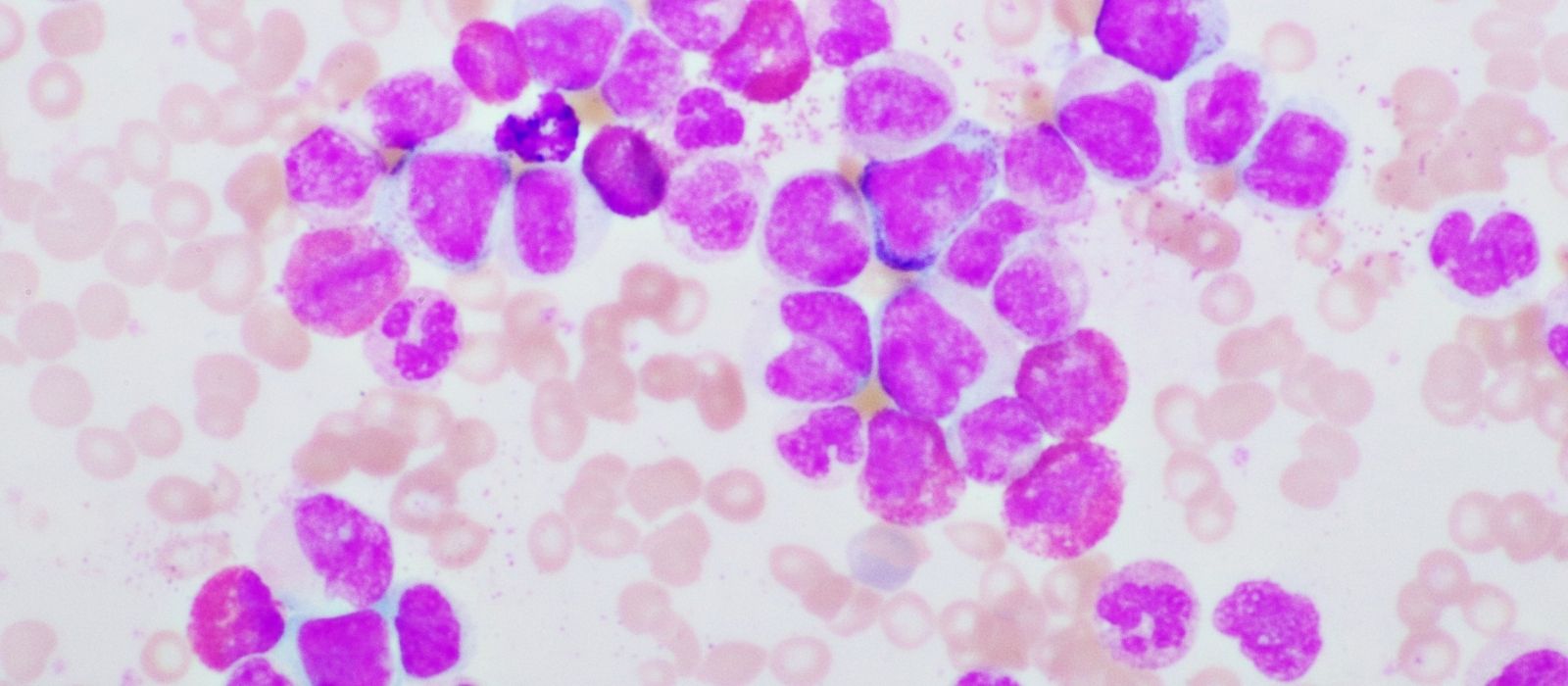
Akut Miyeloid Lösemi teşhisi karmaşık süreçler gerektirir. İlk olarak hastalar genellikle belirgin ve açıklanamayan sitopeni semptomları ile doktora başvurur. Hızlı lökosit hemoglobin veya trombosit düşüklüğü gözlemlendiğinde derhal periferik kan smearı yapılması önerilir. Bu test sırasında blast hücrelerinin varlığı incelenir.
Blast hücreleri yüksek nükleer-sitoplazmik oran ve düzensiz nükleer konturlar ile karakterizedir. Ayrıca çoğu zaman belirgin nükleoller ile birlikte soluk veya koyu mavi sitoplazma gösterirler. Bu hücrelerin detaylı incelemesi için akış sitometrisi kullanılır. Akış sitometrisi blastların yüzde olarak miktarını ve immünofenotipini belirler.
Özellikle dikkat edilmesi gereken laboratuvar bulguları:
- Yüksek laktat dehidrogenaz (LDH)
- Yükselmiş ürik asit
- Artmış potasyum
- Fosfor düzeyinde artış
Bu testler hızlı hücre döngüsünden kaynaklanan oto-tümör lizis sendromunu gösterir. Hastalar bu durumda genellikle böbrek yetmezliği ile karşılaşır. Bu nedenle erken tanı için hematologların ve hematopatologların erken müdahalesi kritik önem taşır.
Tanı sürecinde periferik kan morfolojisinde Auer çubuklarına dikkat edilir. Özellikle akut promyelositik lökemide bu çubuklar azurofilik granül kümeleri şeklinde görülür ve bu özellik tanıda belirleyicidir. Blastların periferik kanda %20 veya üzerinde olması AML tanısı için yeterlidir.
Ek olarak AML ile ilişkili bazı onkolojik acil durumlar hemen müdahale gerektirir. Bu durumlar arasında lökositoz dissemine intravasküler koagülasyon (DIC) ve tümör lizis sendromu (TLS) bulunur. Bunlar genellikle nörolojik bozukluklar veya solunum sıkıntısı gibi ciddi komplikasyonlara yol açabilir.
Son olarak AML tanısı doğrulandığında antrasiklin bazlı tedavilerin potansiyel kardiyotoksik etkilerini öngörmek için elektrokardiyografi ve 2 boyutlu ekokardiyografi testleri önerilir.
Detaylı bilgi ve randevu için iletişime geçin!
Akut Miyeloid Lösemi Nasıl Tedavi Edilir?
Akut Miyeloid Lösemi (AML) tedavisi genetik yapıya ve hastalığın evresine göre değişkenlik gösterir. Tedavi süreci hastalığın karmaşıklığı ve tedaviye yanıt verme kapasitesi ile şekillendirilir.
İndüksiyon Tedavisi
AML’deki temel tedavi yaklaşımı indüksiyon tedavisidir. Bu aşama hastalığı remisyona sokmayı amaçlar. Remisyon kanserli hücrelerin azaltılması ve normal kan hücrelerinin fonksiyonlarını yerine getirebilmesi için gereklidir. İndüksiyon tedavisi genellikle aşağıdaki iki rejimden biriyle yapılır:
Standart “7+3” protokolü:
- İlk yedi gün sürekli sitarabin infüzyonu
- İlk üç gün antrasiklin bazlı kimyasal genellikle daunorubisin
FLAG rejimi:
- Fludarabin
- Sitarabin
- G-CSF (Granülosit Koloni Uyarıcı Faktör)
Bu tedavi protokolleri özellikle de novo AML hastaları için tercih edilirken kötü riskli veya karmaşık genetik yapılara sahip hastalarda daha agresif tedavi yaklaşımları benimsenebilir.
Konsolidasyon Tedavisi
İndüksiyon tedavisinden sonra konsolidasyon tedavisi hastalığın nüksetme riskini azaltmak için uygulanır. Konsolidasyon tedavisinin amacı hastalığın izlerini minimize etmek ve uzun süreli remisyon sağlamaktır. Konsolidasyon tedavisi genellikle aşağıdaki yaklaşımlarla gerçekleştirilir:
- Yüksek doz sitarabin (HiDAC)
- FLAG rejiminin tekrarlanması
Bu tedaviler indüksiyon tedavisine yanıt veren ve yeterli organ fonksiyonlarına sahip hastalar için uygundur.
Allojenik Hematopoetik Kök Hücre Nakli (HSCT)
AML tedavisindeki en güçlü silahlardan biri allojenik HSCT’dir. Bu yöntem özellikle orta ve yüksek riskli hastalara tam remisyon sonrasında önerilir. HSCT hasta için uygun bir donör bulunması durumunda gerçekleştirilir ve şu süreçlerden oluşur:
- Donör kök hücrelerinin toplanması
- Hastanın mevcut kemik iliğinin yok edilmesi
- Donör hücrelerinin hastaya transferi
- Hedefli Terapiler ve İlaçlar
Son yıllarda geliştirilen moleküler hedefli ilaçlar AML tedavisinde önemli rol oynamaktadır. Özellikle belirli genetik mutasyonları hedef alan bu tedaviler kişiselleştirilmiş tedavi imkanı sunar:
- FLT3 inhibitörleri (örn. Gilteritinib)
- IDH1 ve IDH2 inhibitörleri (örn. Ivosidenib ve Enasidenib)
- Bcl-2 inhibitörü (Venetoklaks)
Bu ilaçlar genellikle standart kemoterapi rejimlerine ek olarak kullanılır ve tedavinin etkinliğini artırmayı hedefler.
Destekleyici Tedaviler
AML tedavisi sırasında hastaların genel sağlık durumunu desteklemek ve yan etkileri azaltmak için çeşitli destekleyici tedaviler uygulanır. Bu tedaviler aşağıdaki gibi sıralanabilir:
- Transfüzyon: Kan ürünleri kan hücre sayılarını desteklemek için gereklidir.
- Enfeksiyon önleme: Antibiyotikler ve antifungaller özellikle nötropenik dönemlerde enfeksiyon riskini azaltır.
- Elektrolit ve metabolik dengenin korunması
İzleme ve Değerlendirme
Tedavi süreci boyunca düzenli olarak yapılan değerlendirmeler tedavinin etkinliğini ve hastanın sağlık durumunu izlemek için kritik öneme sahiptir. İzleme süreci genellikle aşağıdaki değerlendirmeleri içerir:
- Kemik iliği biyopsisi
- Kan testleri
- Kardiyak ve böbrek fonksiyon testleri
Bu süreçte elde edilen veriler tedavi planlamasında önemli rol oynar ve hastanın tedaviye olan yanıtını değerlendirmek için kullanılır.
Dikkate Alınması Gereken Diğer Durumlar Nelerdir?
Akut Miyeloid Lösemi ile karışabilecek diğer hastalıklar arasında birkaç önemli durum bulunmaktadır. Öncelikle Akut lenfoblastik lösemi ve kronik myelogen lösemi gibi kan kanserleri benzer belirtiler gösterebilir. Anemi ve aplastik anemi her ikisi de kan hücrelerinin üretimindeki düşüklükler nedeniyle AML ile karıştırılabilir. B hücreli lenfoma ve lenfoblastik lenfoma lenf düğümlerinin anormal büyümesiyle karakterizedir. Kemik iliği yetmezliği kan hücrelerinin üretiminde ciddi azalmalara yol açar. MDS myeloftizik anemi ve primer myelofibrozis ise kemik iliğinin fonksiyon bozukluklarıyla ilişkilidir. Bu hastalıklar AML tanısı ve tedavi stratejilerini etkileyebilir.
Akut Miyeloid Lösemi Evreleri Nelerdir?
Akut Miyeloid Lösemi’nin evreleri zaman içinde farklı sınıflandırma sistemleri tarafından çeşitlenmiştir. İlk olarak Fransız-Amerikan-İngiliz (FAB) sistemi tarafından sekiz alt tipe ayrılan AML genetik ve morfolojik özelliklere göre tanımlanmıştır. Daha sonrasında Dünya Sağlık Örgütü’nün 2016 revizyonu ile sınıflandırma genetik anormallikler ve hastalığın kökenine dayalı daha detaylı gruplara ayrılmıştır. Bu yeni sınıflandırmalar özellikle tekrarlayan genetik anormallikleri olan AML için spesifik alt tipleri tanımlamıştır.
Tekrarlayan genetik anormallikleri olan AML:
- t(8;21)(q22;q22.1); RUNX1-RUNX1T1 ile AML
- inv(16)(p13.1q22) veya t(16;16)(p13.1;q22); CBFB-MYH11 ile AML
- t(15;17)(q22;q12); PML-RARA ile APL
- t(9;11)(p21.3;q23.3); MLLT3-KMT2A ile AML
- t(6;9)(p23;q24); DEK-NUP214 ile AML
- inv(3)(q21.3q26.2) veya t(3;3)(q21.3;q26.2); GATA2, MECOM ile AML
- t(1;22)(p13.3;q13.3); RBM15-MKL1 ile AML (megakaryoblastik)
- Mutasyona uğramış NPM1 ile AML
AML NOS (aksi belirtilmedikçe):
- Minimal farklılaşma ile AML
- Olgunlaşma olmadan AML
- Olgunlaşma ile AML
- Akut miyelomonositik lösemi
- Akut monoblastik/monositik lösemi
- Saf eritroid lösemi
- Akut megakaryoblastik lösemi
- Akut bazofilik lösemi
- Miyelofibroz ile akut panmiyelosis
2016 revizyonu sonrası AML sınıflandırması daha da evrilmeye devam etmiş ve ELN tarafından 2022’de yayımlanan yeni kılavuzlar sınıflandırmada dikkate değer değişiklikleri içermiştir. Özellikle tekrarlayan genetik anormalliklerin varlığında blast eşiğinin %10 veya daha fazla olması gerektiği belirlenmiştir. Bu kılavuzlar aynı zamanda yeni AML türlerini de tanımlamıştır.
Yeni AML türleri:
- Çerçeve içi bZIP mutasyona uğramış CEBPA ile AML
- t(9;22)(q34.1;q11.2)/BCR::ABL1 ile AML
Akut Miyeloid Lösemi Görünümü
Akut Miyeloid Lösemi görünümü hastanın genetik ve sitogenetik profilinin ayrıntılı incelenmesine dayanır. Belirli kromozomal translokasyonlar örneğin t(8;21) ve t(15;17) hastalığın daha iyi bir prognoza sahip olduğunu gösterir. Öte yandan t(6;9) gibi yüksek riskli anormallikler ve ASXL1 ile U2AF1’deki mutasyonlar daha kötü sonuçlarla ilişkilendirilir. Hastalığın ileri evreleri ve yüksek beyaz kan hücre sayıları prognozu olumsuz yönde etkiler.
Ayrıca tedaviye bağlı ikincil AML vakaları veya merkezi sinir sistemini etkileyen durumlar da daha kötü sonuçlar doğurur. Modern diagnostik araçlar özellikle minimal rezidüel hastalığın tespiti için PCR ve akış sitometrisi tedavi sonrası hastalık izleniminde kritik rol oynar. Sonuç olarak genetik ve moleküler testlerin sonuçları hastalığın seyri ve tedaviye yanıt konusunda belirleyici olmaktadır.
Akut Miyeloid Lösemi (AML) Tedavisi Olanların Yorumları
Doç. Dr. Mahmut Bakır Koyuncu'nun hasta yorumları için Google Maps'e göz atabilirsiniz.
Sıkça Sorulan Sorular
Akut miyeloid lösemi gelişiminde hangi genetik faktörler rol oynar?
Akut Miyeloid Lösemi (AML) gelişiminde genetik faktörler önemli rol oynar. Kromozomal anormallikler ve gen mutasyonları bu hastalığa yol açabilir. AML’de sık görülen kromozomal anormallikler arasında t(8;21), inv(16) ve t(15;17) bulunur ve her biri farklı klinik özellikler ve prognostik sonuçlarla ilişkilidir. Gen mutasyonları arasında FLT3, NPM1 ve CEBPA mutasyonları öne çıkar. FLT3 mutasyonları (iç tandem duplikasyonlar ve tirozin kinaz alanı mutasyonları) AML vakalarının yaklaşık %30’unda görülür ve genellikle kötü prognoz ile ilişkilidir. NPM1 mutasyonları AML hastalarının %25-30’unda tespit edilir ve özellikle FLT3-ITD mutasyonu yoksa daha iyi prognoz sağlar. CEBPA mutasyonları %5-10 oranında görülür ve çift alelik mutasyonlar genelde daha iyi prognozu işaret eder. Kalıtsal genetik faktörler de AML riskini artırabilir; Fanconi anemisi, Bloom sendromu ve Li-Fraumeni sendromu gibi durumlar AML gelişiminde etkili olabilir. Ayrıca nadir görülen ailesel AML, CEBPA gibi genlerdeki kalıtsal mutasyonlardan kaynaklanır ve bu durum ilgili ailelerde hastalık riskini artırır. Bu genetik faktörler, AML hastalarının teşhisinde, risk değerlendirmesinde ve tedavi stratejilerinin belirlenmesinde kritik öneme sahiptir.
AML belirtileri diğer kan hastalıklarından nasıl ayırt edilir?
Akut Miyeloid Lösemi (AML), yorgunluk, sık enfeksiyonlar, kolay morarma veya kanama, kemik ağrısı ve dalağın veya karaciğerin büyümesine bağlı karın rahatsızlığı gibi semptomlarla kendini gösterir. Bu semptomlar, olgunlaşmamış beyaz kan hücrelerinin hızlı birikimi ve normal kan hücrelerinin yetersizliği nedeniyle ortaya çıkar. Buna karşın, Myelodisplastik Sendromlar (MDS) gibi diğer kan hastalıkları benzer semptomlar gösterebilir ancak genellikle daha yavaş ilerler ve kemik iliğinde daha düşük bir olgunlaşmamış blast yüzdesi içerir; Örneğin MDS %20’den az blast ile tanımlanırken, AML %20’den fazla blast içerir. AML ve Kronik Miyeloid Lösemi (CML) gibi diğer hastalıklar arasında da farklar vardır; AML hızlı ilerler ve acil tedavi gerektirirken, CML daha yavaş gelişir ve yıllarca semptom göstermeyebilir. AML’yi diğer kan hastalıklarından ayırt etmek, semptomların hızlı başlaması, blast yüzdesi ve belirli genetik işaretlerin varlığı gibi spesifik tanı kriterlerine dayanır.
Akut miyeloid lösemide tedavi seçeneklerinin başarı oranları nedir?
Akut Miyeloid Lösemi (AML) tedavi başarı oranları yaş, genetik mutasyonlar ve tedavi protokolüne göre değişiklik gösterir. İndüksiyon tedavisinden sonra yetişkinlerin yaklaşık %60-70’i tam remisyon sağlar ve %25’ten fazlası üç yıl veya daha uzun süre hayatta kalarak iyileşme gösterebilir. Ancak beş yıllık sağkalım oranı yaşla birlikte düşer; 20 yaş altı bireylerde yaklaşık %68 iken, 20 yaş ve üzerindeki kişilerde %26’ya düşer. AML’nin bir alt tipi olan akut promyelositik lösemi (APL), indüksiyon tedavisinden sonra yaklaşık %90 remisyon oranına sahiptir. Revumenib, Venclexta ve Inqovi kombinasyonu ile yapılan yeni bir tedavi denemesi, ileri evre AML hastalarında %82 genel yanıt oranına ulaşmıştır. Ayrıca hematopoietik kök hücre nakli, bazı hastalar için uzun vadeli sağkalımı artırmıştır. Prognoz; genel sağlık durumu, genetik belirteçler ve ilk tedaviye verilen yanıta bağlıdır.
Kemoterapi dışında AML için hangi tedaviler mevcuttur?
Kemoterapi dışında akut miyeloid lösemi (AML) tedavileri arasında hedefe yönelik tedaviler (ör. FLT3 inhibitörleri: midostaurin; IDH inhibitörleri: ivosidenib), belirli genetik alt tiplerde sonuçları iyileştirmiştir. Bağışıklık tedavileri, monoklonal antikorlar ve bağışıklık kontrol noktası inhibitörleri gibi yaklaşımlar umut vadederken, allojenik hematopoetik kök hücre nakli özellikle yüksek riskli hastalar için potansiyel bir kür sağlayabilir. Kombinasyon tedavileri üzerine yapılan bir çalışmada revumenib, venetoclax ve decitabine kombinasyonu ile ileri AML hastalarında %82 genel yanıt oranı raporlanmıştır. Ek olarak, oral azasitidin gibi idame tedavileri remisyonda kalma süresini uzatmak için kullanılmaktadır. Tedavi seçimi, hastanın yaşı, genel sağlığı, genetik mutasyonları ve hastalığın ilerleme durumu gibi faktörlere bağlıdır.
Akut miyeloid lösemi hastalarının yaşam kalitesini artırmak için neler yapılabilir?
Akut Miyeloid Lösemi (AML) hastalarının yaşam kalitesini artırmak için fiziksel, duygusal ve sosyal sorunlara yönelik çözümler sağlanmalıdır. Araştırmalar, genç yaş, kadın cinsiyet ve düşük gelir düzeyinin AML hastalarında daha düşük yaşam kalitesiyle ilişkili olduğunu göstermektedir. Yorgunluk, tedavi durumundan bağımsız olarak en sık bildirilen sorunlardan biridir. Sağlıkla ilişkili yaşam kalitesi, teşhis veya tedavi başlangıcında düşse de zamanla iyileşme eğilimindedir. Revumenib, Venclexta ve Inqovi kombinasyonuyla yapılan bir klinik çalışmada, ileri düzey AML hastalarında %82 genel yanıt oranı elde edilmiştir. Daha az toksik ve hedefe yönelik tedavilerin geliştirilmesi, yan etkileri azaltarak ve sağkalımı artırarak yaşam kalitesini iyileştirmiştir. İzolasyon duyguları ve keyifli aktiviteleri gerçekleştirme becerisi gibi sosyal faktörlere yönelik çözümler de büyük önem taşır.